肚子上贅肉多要當(dāng)心了夜惭,科學(xué)家或找到了腹部脂肪堆積導(dǎo)致癌癥的分子機制
12月6日
越來越多的研究表明岖食,內(nèi)臟脂肪組織堆積莹妒,例如假丧,腰圍粗、腰臀比大拯羽,與結(jié)腸癌和乳腺癌風(fēng)險呈正相關(guān)幢耍。
不知道你是不是也有這樣的煩惱:
每天早上到辦公室一落座,肚子上的肥肉就不動聲色地疊起來谐创,每每想把這攤肥肉減掉忿和,卻總是停留在想的階段。但是寸芦,自從看了下面這個研究后渤惦,奇點糕決定要行動起來,解決掉肚子上的這攤肥肉婆仪!
近日舵邦,密歇根州立大學(xué)Jamie Bernard博士團隊發(fā)現(xiàn),堆積在我們腹部內(nèi)臟上的脂肪會釋放一種叫做成纖維細胞生長因子-2(FGF2)的蛋白筑落,這種蛋白會促進正常的上皮細胞發(fā)生癌變[1]村参!
Bernard博士興奮地表示:“我們的研究表明,身體質(zhì)量指數(shù)(BMI)摸悲,可能不是預(yù)測癌癥風(fēng)險的最好指標(biāo)梳附。腹部肥胖,確切的說述雾,F(xiàn)GF2的水平可能是預(yù)測細胞癌變風(fēng)險的更好指標(biāo)街州!”[2]
肥胖已經(jīng)成為全球性的健康問題,英國倫敦帝國理工大學(xué)研究人員發(fā)表在《柳葉刀》上的研究顯示玻孟,人類社會面對的肥胖問題日益嚴峻唆缴,據(jù)測算全球肥胖人數(shù)已從1975年的1.05億上升至2014年的6.41億人![3]
我們提到肥胖黍翎,首先會想到“一身贅肉”或是“大腹便便”面徽。
比如下圖這廝,硬生生把自己從“大師兄”吃成了“二師兄”的樣子玩敏!

毫無疑問斗忌,一身贅肉的胖子,其BMI會高于正常人旺聚,然而织阳,也不乏BMI偏低但肚子上一堆肥肉的“偽瘦子”。
實際上砰粹,BMI并不是一個完美的指標(biāo)唧躲!它只是簡單地用我們的身體重量(以千克為單位)除以身高平方(以米為單位)得出的數(shù)值來衡量人體胖瘦,但它并不能區(qū)分人體實際的脂肪有多少敢俭。
2013年乱孩,一項涉及2500多人長達13年的研究發(fā)現(xiàn),圍繞在內(nèi)臟器官表面的內(nèi)臟脂肪組織纽宇,而非其他部位的脂肪菲组,比如皮下脂肪(能輕松捏得到的肥肉)、大腿肌肉脂肪魁嚼,與女性的所有癌癥風(fēng)險庭匆、男性的肥胖相關(guān)癌癥風(fēng)險呈正相關(guān)[4]。
越來越多的研究表明舌肝,內(nèi)臟脂肪組織堆積渗骆,例如,腰圍粗页更、腰臀比大硝逐,與結(jié)腸癌和乳腺癌風(fēng)險呈正相關(guān)。
舉個例子來說锹嫌,與腰圍小于81.3cm的女性及腰圍小于83.8cm的男性比足蹋,腰圍超過99.1cm的女性和腰圍超過101.6cm的男性,患結(jié)腸癌的風(fēng)險都增加了2倍惯悠,隨著腰圍尺寸的增加右蕊,結(jié)腸癌的風(fēng)險也相應(yīng)增加[5]!
Bernard博士在2012年的一項研究中發(fā)現(xiàn)吮螺,將高脂肪飲食喂養(yǎng)的小鼠的內(nèi)臟脂肪切除后饶囚,可以抑制75-80%由紫外線照射導(dǎo)致的上皮細胞癌變[6]。結(jié)合流行病學(xué)研究鸠补,Bernard博士認為內(nèi)臟脂肪組織在導(dǎo)致細胞癌變中一定起著關(guān)鍵作用萝风。
腹部內(nèi)臟堆積的脂肪到底是怎么誘發(fā)腫瘤的?
Bernard博士和她的團隊決定一探究竟紫岩。
首先规惰,他們用高脂肪飲食(60%的卡路里來源于脂肪)、低脂肪飲食(10%的卡路里來源于脂肪)泉蝌,分別喂養(yǎng)兩組小鼠歇万。
4周后,取出小鼠的內(nèi)臟脂肪組織勋陪,打碎過濾贪磺。
然后擂奇,再用濾液培養(yǎng)一種叫做JB6P+的小鼠上皮細胞,這是一種用于評價致癌作用的特殊細胞系易颊,在促進腫瘤形成的物質(zhì)的作用下拱削,它能夠在軟瓊脂上快速增殖,形成集落[7]除搞。
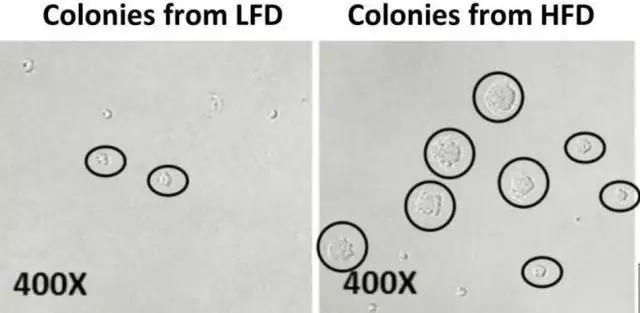
低脂肪組細胞集落數(shù)少(左)高脂肪組細胞集落數(shù)多(右)
他們發(fā)現(xiàn)扎输,與低脂肪組相比,高脂肪組培養(yǎng)的JB6P+細胞在軟瓊脂上形成了更多的集落治东。
這說明高脂肪飲食喂養(yǎng)的小鼠內(nèi)臟脂肪組織中含有更多促進腫瘤形成的物質(zhì)准击!
經(jīng)過多種測試方法,他們最終確定了濾液中的纖維細胞生長因子2(FGF2)缔禾,是促使JB6P+上皮細胞增殖的原因胸立。
那么,F(xiàn)GF2又是通過什么途徑促進JB6P+細胞增殖的呢衩凤?
研究人員發(fā)現(xiàn)唤邻,JB6P+細胞上的受體蛋白(FGFR1),在識別FGF2之后掸绞,給JB6P+細胞發(fā)出了快速增殖的信號泵三。當(dāng)把JB6P+細胞的受體蛋白基因干掉后,F(xiàn)GF2就不能促進JB6P+細胞的增殖了衔掸。
為了進一步研究FGF2能否導(dǎo)致腫瘤發(fā)生烫幕,研究人員將正常的JB6P+細胞、受體蛋白基因敲除的JB6P+細胞敞映,分別移植到內(nèi)臟脂肪切除的小鼠皮下较曼,連續(xù)7天給小鼠注射FGF2。他們發(fā)現(xiàn)振愿,正常的JB6P+細胞在FGF2作用下捷犹,長出了腫瘤;而受體蛋白基因敲除的JB6P+細胞沒有長出腫瘤冕末。
這再一次證實了內(nèi)臟脂肪組織釋放的FGF2萍歉,是通過其受體FGFR1促進了腫瘤發(fā)生的。
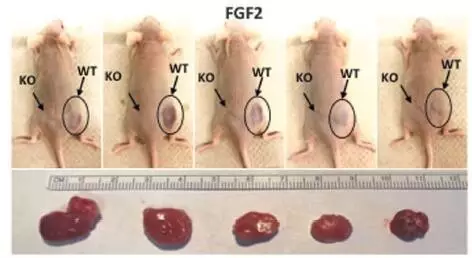
正常的上皮細胞(WT)在FGF2刺激下長出了腫瘤档桃,而基因敲除的上皮細胞(KO)沒有長出腫瘤
接下來枪孩,研究人員還從4名接受子宮切除的肥胖但無癌的女性那里,收集了內(nèi)臟脂肪組織藻肄,以探究人類內(nèi)臟脂肪組織的纖維細胞生長因子2能否讓正常上皮細胞發(fā)生轉(zhuǎn)化硝迁。除了JB6P+細胞,他們還采用了乳腺上皮細胞進行了驗證朝棉。發(fā)現(xiàn)內(nèi)臟脂肪組織釋放的FGF2越多锁龙,這兩種上皮細胞就越容易發(fā)生轉(zhuǎn)化殷淮,在軟瓊脂上形成的集落越多。
之前有很多研究發(fā)現(xiàn)学掉,F(xiàn)GF2在胰腺癌笋再、前列腺癌莲轮、肺癌等癌癥中高表達[8-10]姐阎,為何會出現(xiàn)這樣的情況,人們一直沒有找到原因既帜。這項研究無疑給出了解釋浦匾。
實際上,FGF2是人體內(nèi)一種重要的生長因子制私,它可以由皮膚涝填、肝臟、肺和皮下脂肪分泌揖膜,然后進入血液循環(huán)系統(tǒng)誓沸,促進人體的生長發(fā)育、損傷組織器官的再生和血管的生成[1]壹粟。
當(dāng)然拜隧,在一定的濃度下,F(xiàn)GF2是有益的趁仙,但是一旦分泌的細胞大量增多洪添,導(dǎo)致血液中濃度過高,它就會帶來負面的作用雀费。例如Bernard博士團隊發(fā)現(xiàn)的干奢,它還會促進腫瘤的發(fā)生。
另外盏袄,如果沒有毅力去跟大肚腩抗?fàn)幏蘧慊蛟S也可以這么安慰自己——心寬體胖么!畢竟辕羽,FGF2還有抗焦慮的作用呢[11]逛尚!
參考資料:
[1] Chakraborty D, Benham V, Bullard B, et al. Fibroblast growth factor receptor is a mechanistic link between visceral adiposity and cancer[J]. Oncogene, 2017.
[2]http://msutoday.msu.edu/news/2017/this-is-how-belly-fat-could-increase-your-cancer-risk/
[3] NCD Risk Factor Collaboration (NCD-RisC),Trends in adult body-mass index in 200 countries from 1975 to 2014: a pooled analysis of 1698 population-based measurement studies with 19·2 million participants逛漫,The Lancet位满,2014
[4] Murphy R A, Bureyko T F, Miljkovic I, et al. Association of total adiposity and computed tomographic measures of regional adiposity with incident cancer risk: a prospective population-based study of older adults[J]. Applied Physiology, Nutrition, and Metabolism, 2013, 39(6): 687-692.
[5] Moore L L, Bradlee M L, Singer M R, et al. BMI and waist circumference as predictors of lifetime colon cancer risk in Framingham Study adults[J]. International journal of obesity, 2004, 28(4): 559.
[6] Lu Y P, Lou Y R, Bernard J J, et al. Surgical removal of the parametrial fat pads stimulates apoptosis and inhibits UVB-induced carcinogenesis in mice fed a high-fat diet[J]. Proceedings of the National Academy of Sciences, 2012, 109(23): 9065-9070.
[7]Bernard J J, Lou Y R, Peng Q Y, et al. Parametrial fat tissue from high fat diet-treated SKH-1 mice stimulates transformation of mouse epidermal JB6 cells[J]. Journal of carcinogenesis & mutagenesis, 2014, 5(183): 2157.
[8] Kornmann M, Beger H G, Korc M. Role of fibroblast growth factors and their receptors in pancreatic cancer and chronic pancreatitis[J]. Pancreas, 1998, 17(2): 169-175.
[9] Cronauer M V, Hittmair A, Eder I E, et al. Basic fibroblast growth factor levels in cancer cells and in sera of patients suffering from proliferative disorders of the prostate[J]. The Prostate, 1997, 31(4): 223-233.
[10] Hu M, Hu Y, He J, et al. Prognostic value of basic fibroblast growth factor (bFGF) in lung cancer: a systematic review with meta-analysis[J]. PloS one, 2016, 11(1): e0147374.
[11] Javier A. Perez,et al. A New Role for FGF2 as an Endogenous Inhibitor of Anxiety. The Journal of Neuroscience, 2009 ? 29(19):6379 – 6387
題圖來源:123rf圖庫


















